@Jayfeather
2018-05-09T12:50:32.000000Z
字数 6239
阅读 2416
分析化学复习讲义
课程
By Jayfeather
第一章
分析化学的定义
分析化学是以发展并运用各种方法、仪器及策略,并在时间和空间的维度里获得有关物质组成及其性质的信息的一门科学。化学分析 VS 分析化学
化学分析特别指针对日常样品进行的日常分析。
分析化学改进现有的方法、拓展现有的方法于新的样品,以及发展新的方法去测量新的化学现象。化学分析法的优缺点
优点 —– 具有严格的定量理论基础,属绝对定量分析方法。
缺点 —– 通常只适用于单组分常量分析,操作步骤较多。仪器分析法的优缺点
优点 —– 高灵敏度、高精密度、高信息量、多组分同时定量分析、操作简便等。
缺点 —– 非绝对定量分析方法,需要待测物的标准品建立校正曲线才能实现定量分析。
第二章
- 滴定分析法
滴定分析法是通过测量物质之间定量反应完全之后所消耗的标准试剂的体积来进行定量分析的方法。
滴定分析法运用化学反应的计量关系来实现定量分析。
滴定分析法是重量分析法的某种形式的拓展或延伸。 滴定分析法的条件
1 滴定反应必须有确定的化学计量关系。
2 滴定反应有较快的反应速度。
3 必须有合适的方法确定化学计量点。物质的量浓度
物质的量浓度是以物质的基本单元为基准构建的一种浓度表达方式,这个基本单元可以是实际的物质组成形式,也可以是人为定义的物质组成形式。质量平衡例题
定量分析 时,先将其灼烧生成,然后通过与 反应生成 。生成的 用 NaOH 滴定,消耗浓度为 0.02500mol/L 的 NaOH 溶液 34.85 mL,反应式如下:
已知最初样品的质量为0.4613g。求样品中 的含量。
解答:
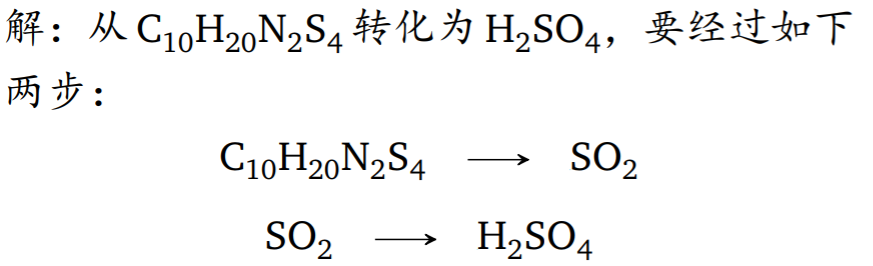
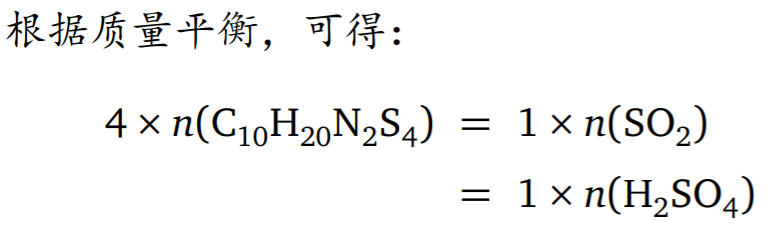
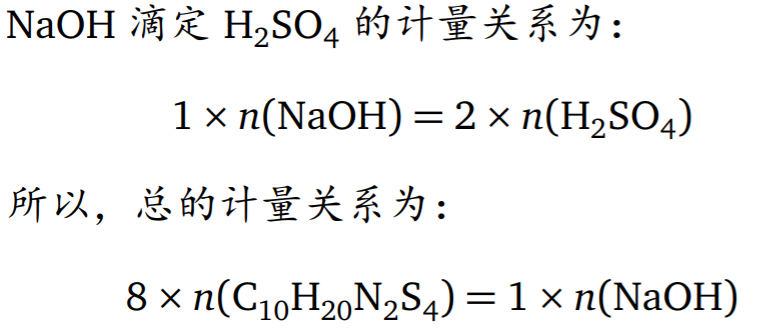
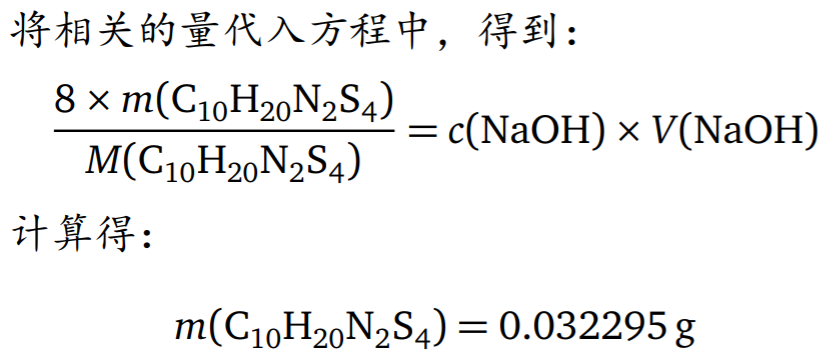

- 基准物质
满足如下条件的物质,可以作为基准物质,直接用于标准溶液的配制。
1 基准物质的组成与化学式完全相符。如果该物质含有结晶水,其结晶水的含量应与化学式相符;
2 基准物质的主成分的含量应在 99.9% 以上;
3 基准物质应有很好的稳定性,不易与空气中的物质发生化学反应,也不易吸附空气中的物质;
4 基准物质的摩尔质量要大。
常用的基准物质
1 纯金属 — Ag,Cu,Zn,Cd,Si,Ge,Al,Co,Ni,Fe 等。
2 化合物 — NaCl,K2Cr2O7,Na2CO3,As2O3,
CaCO3,邻苯二甲酸氢钾,硼砂等。直接配制法
- 用天平准确称取 一定量的某种基准物质;
- 将基准物质溶解于适量水(或酸)中;
- 将溶液定量转入容量瓶中并定容至刻度;
- 根据称取的质量数及容量瓶的体积,计算标准溶液的浓度。
间接配制法
- 将目标物配制成所需浓度近似值的溶液;
- 用基准物对该溶液进行标定;
- 根据消耗基准物的量,计算目标溶液的准
确浓度值
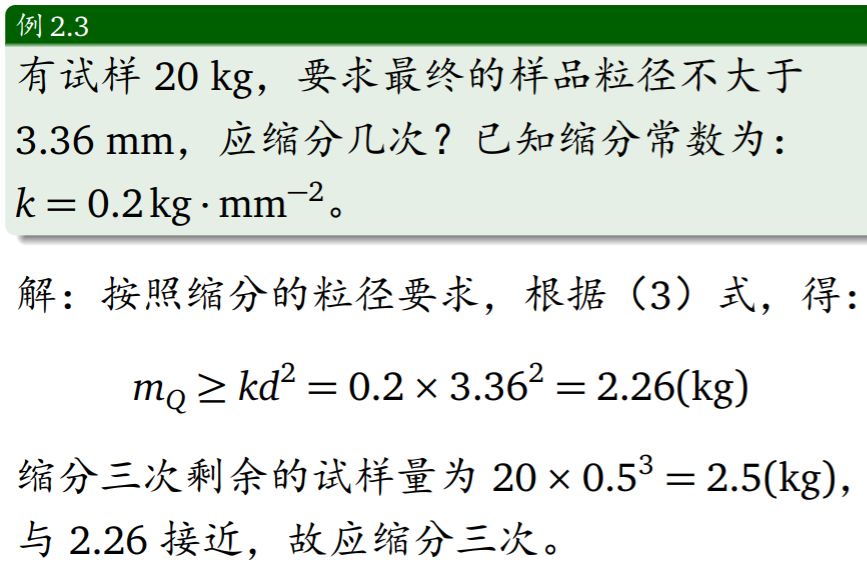
例题

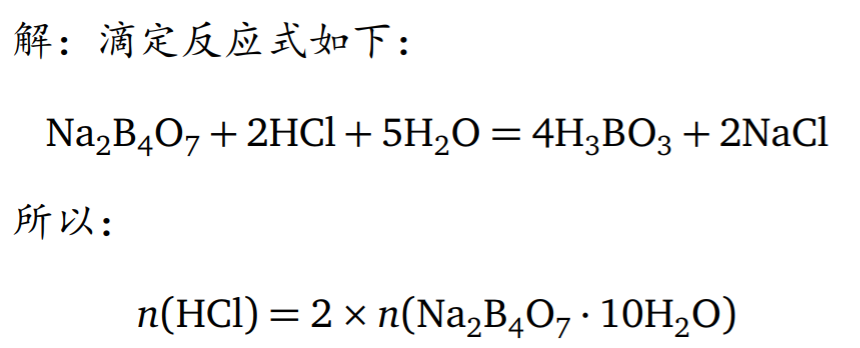

所需样品最小质量
- 是所需试样的最小质量(单位kg)
- d 为试样的最大粒径(单位mm)
- k 是缩分常数,通常取值范围为0.05 ∼ 1 kg · mm
- 样品的测量
- 当组分含量在50%∼100%的范围内时,要求测量的相对误差为0.1%∼0.3%,重量分析法和滴定分析法都可满足这一要求。
- 当组分含量在 0.01% ∼ 1% 的范围内时,对
准确度的要求可放宽至相对误差为2%∼10%,此时宜采用仪器分析法。
第三章
- 真值与测量值
真值 — 任何物质都是一个真实的存在,都有一个确定无疑的、不以人的意志为转移的属性值(如质量),我们称此属性值为真值,通常用 µ 表示。
测量值 — 对物质的属性值进行测量,得到一个描述该属性值的数值,称为测量值,通常用x表示。测量值是对真值的一个估计。 - 有效数字
有效数字 是指实际上能测量到的数字,它包括全部准确测定的数值以及最后一位估计的数值。 - 有效数字概念
测量值受到测量器具的量度误差的制约,必须表达成有效数字形式。
有效数字表达了测量过程的不确定度。
不确定度表达了测量结果可能值的合理范围。
- 有效数字的位数


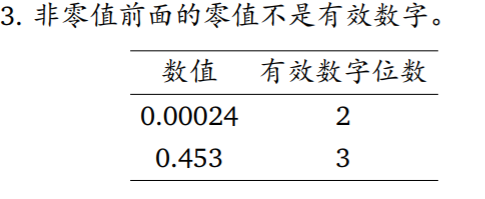

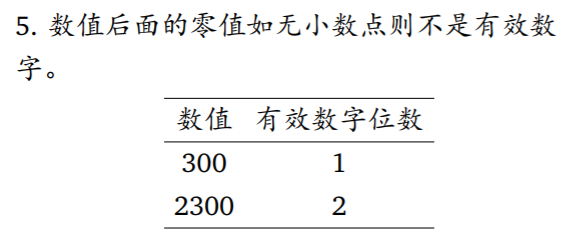
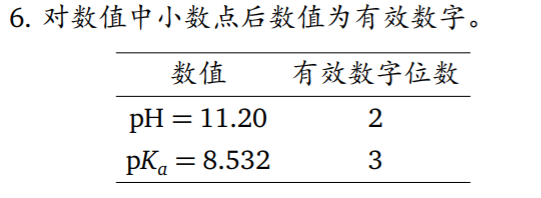
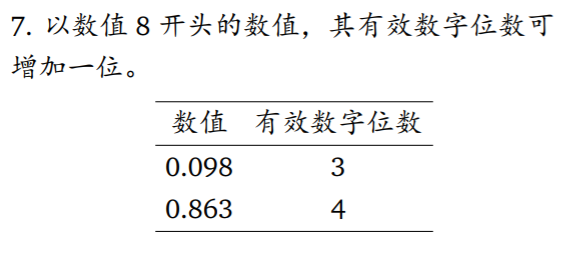

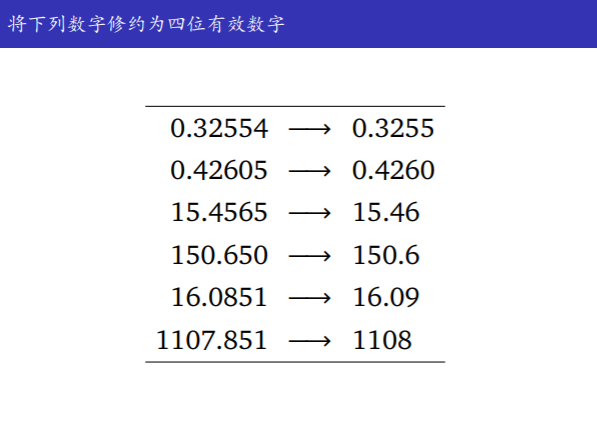
-有效数字的运算规则
加减运算 — 在加减法运算中,最终结果的有效数字位数由其中的小数点后位数最少的数值决定。
乘除运算 — 按照所有数值中有效数字位数最少的数值的有效数字位数来确定最终结果的有效数字位数。


- 随机误差的特点
随机误差可正、可负。
随机误差的取值不确定。不同的测量值中包含的随机误差的大小不同。 - 系统误差的特点
在重复性条件下2系统误差会重复出现且具有相同的值;
系统误差具有单向性,即要么大于零,要么小于零;
系统误差通常可通过标准物质进行校正。 - 绝对误差与准确度
总误差反映了测量值与真值之间真实的差
异,通常也被称为绝对误差,表示如下:
测量值与真值的接近程度称为准确度,衡量准确度的数值指标是绝对误差。 - 95% 置信水平的频率解释
每次得到的每个样本观测值是不同的,从而每次得到的区间也是不一样的。对一次具体的观察值而言,真值可能在上述区域内,也可能不在。平均而言,在这些大量的区间观察值中,至少有95%包含了真值。 - 误差传递




- Grubbs 统计量



- t检验法
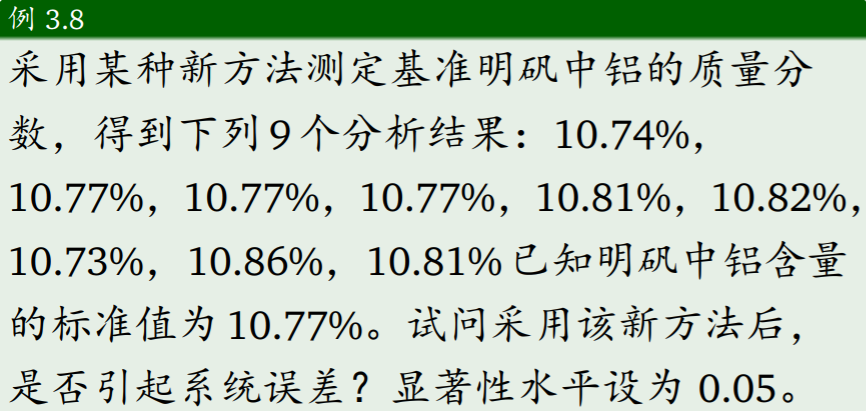
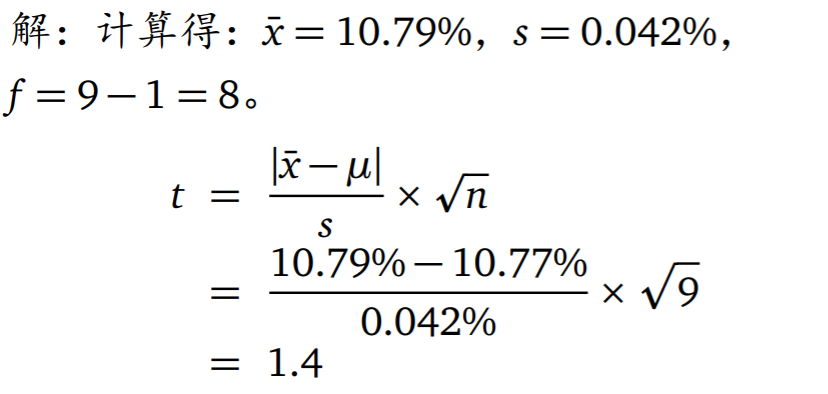

- f检验法
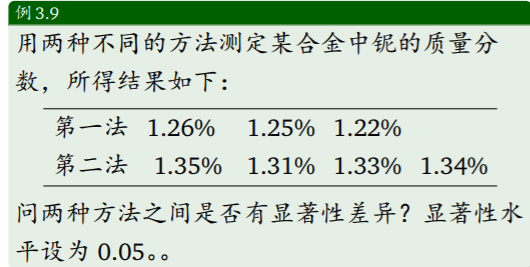



第四章
- 共轭酸碱对
酸失去质子后反而成为了可接受质子的碱,而碱得到质子后又成为了可失去质子的酸,由此引入了共轭酸碱对的概念。 - 分布分数
定义分布分数来描述溶液中酸的各种型体的存在比例。
- 草酸分布分数
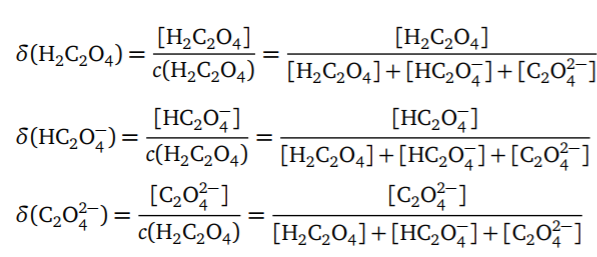
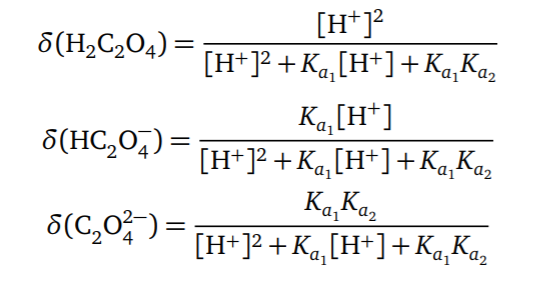
- 草酸分布分数
- 磷酸分布分数
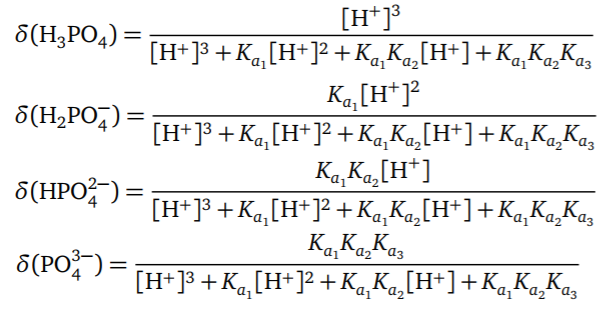
段落引用
- 质子条件式(需要练习)
- 酸碱反应的实质是物质间质子转移;
- 在酸碱反应达到平衡时,酸碱溶液体系中各种物质型体之间存在着一个确定的定量关系,称为质子条件
建立酸碱溶液体系中的质子条件通常有两种方法:
1. 由酸碱溶液中的物料平衡和电荷平衡列出质子条件;
2. 由酸碱溶液中的得失质子关系列出质子条件。(高中内容)(放在这仅仅是告诉你有质子条件式这个东西)
- 缓冲指数与缓冲范围
- 当向缓冲溶液中加入少量酸(或者碱)时,缓冲溶液可以防止溶液的 pH 值发生显著的改变。
- 缓冲溶液防止溶液pH值发生显著改变的能力称为缓冲指数。
- 缓冲指数用 β 表示,其定义为:
这里 是使溶液的 pH值发生dpH改变时
加入的碱的量。
- 缓冲溶液的选择原则
- 缓冲溶液对测量过程应没有干扰。
- 构成缓冲溶液的弱酸的pKa值应尽量与所需控制的 pH 值接近。
- 缓冲溶液应有足够的缓冲容量。
- 酸碱滴定方程
酸碱滴定过程中,溶液的pH值会随着滴定剂的加入而发生改变,因而可以将滴定剂的加入量与溶液体系的pH建立数量关系,这就是滴定方程。 - 强碱滴定强酸



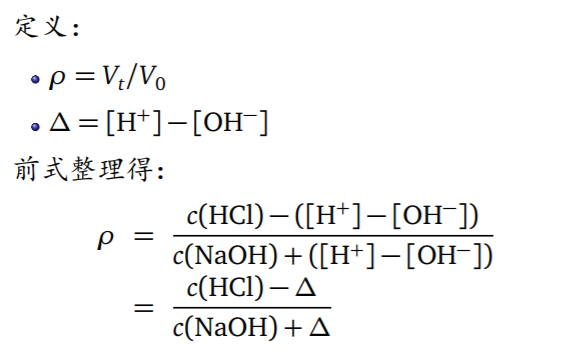
- 化学计量点
滴定的化学计量点是指
时的状态。
化学计量点时的体积比为:
- 滴定突跃范围
等浓度滴定时滴定突跃是指 ρ ∈[0.999 ∼ 1.001] 的范围。
在滴定突跃范围内,酸碱滴定的完成率在99.9% ∼ 100.1%,这意味着滴定误差小于0.1%。
滴定突跃范围是选择指示剂的理论基础。 - 强碱滴定弱酸

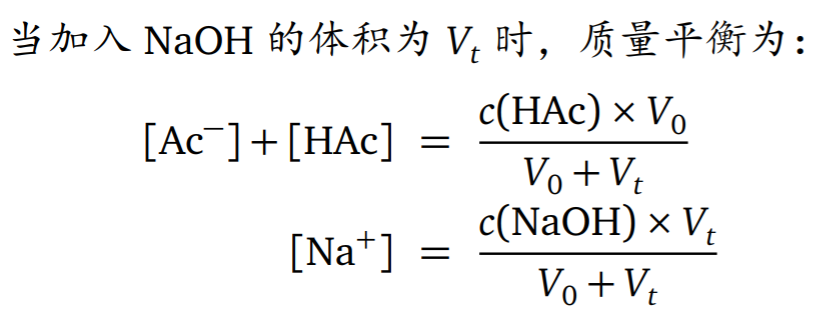

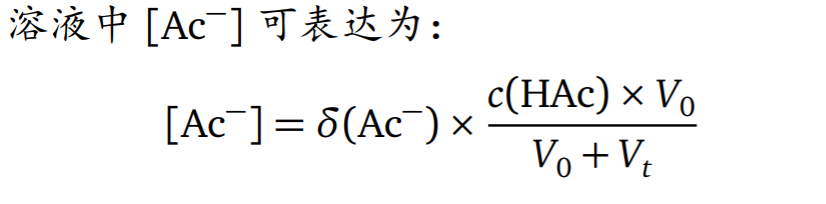
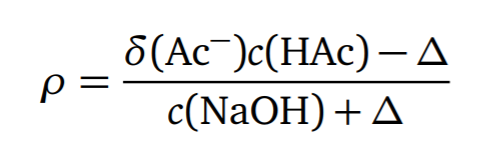
- 强碱滴定多元酸

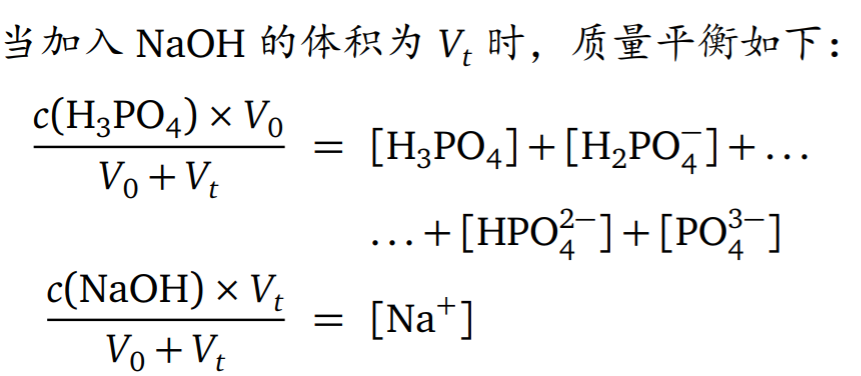
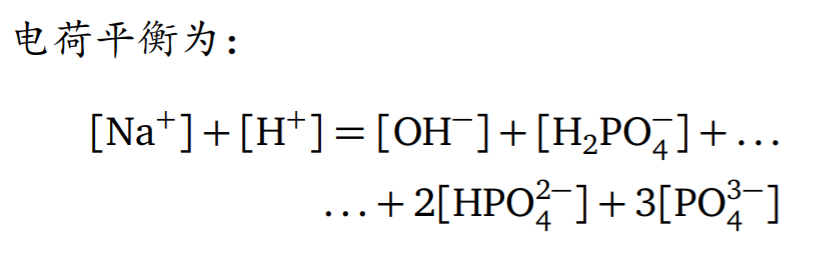

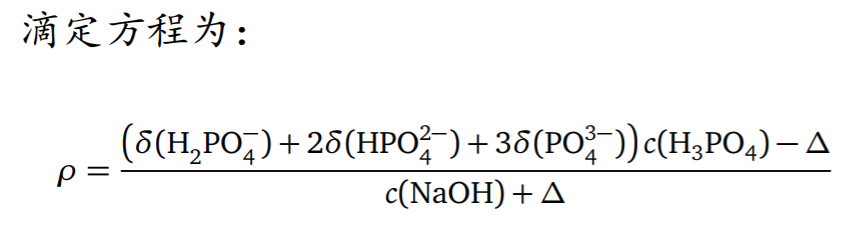
( 要求:会推导公式 计算应该不作要求…… )
- 酸碱指示剂的作用原理
酸碱指示剂是包含有双键结构和苯环结构的有机弱酸或有机弱碱,通常显现出一定的颜色。
当酸碱溶液中的氢离子结合到酸碱指示剂上时,指示剂的结构发生改变,从而导致其颜色的改变。
一般定义指示剂的变色范围为:
- 酸碱滴定误差
在酸碱滴定进程中,当指示剂的颜色发生改变时提示我们终止滴定,此时我们称滴定达到滴定终点。
滴定终点与化学计量点往往并不重合,由此导致滴定剂的消耗量不同,从而产生滴定误差。



- 例题








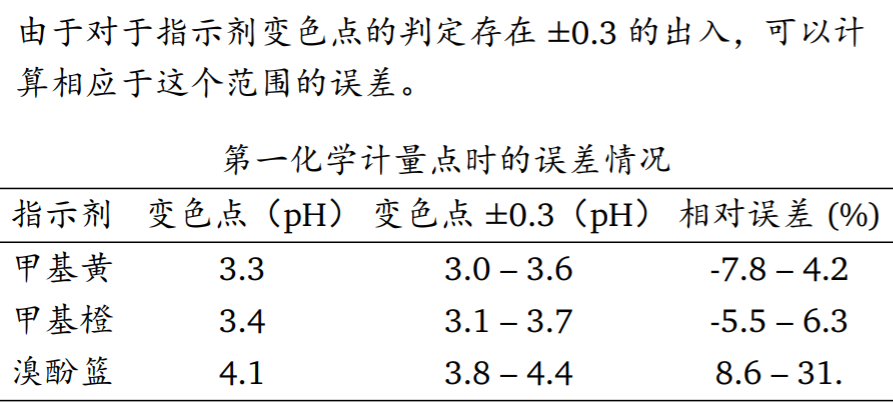
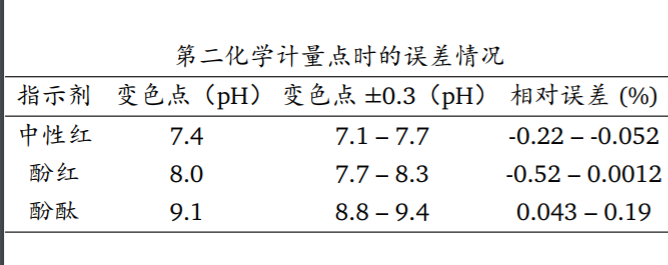
(前面一个例题都没有,这里突然出现这么多?难道没有预示着什么?你的脑海里难道没有听见老师敲着黑板大声说:同学们,这是重点)
-酸碱指示剂的影响
酸碱滴定中采用的指示剂本身是弱酸(或弱碱),它们在滴定过程中必然会参与到滴定过程中,这自然会引发如下两个问题:(1)酸碱指示剂是以一种怎样的方式影响到滴定过程?(2)在实际的滴定过程中究竟应该加入多少指示剂?
用 0.1000 mol/L 的 NaOH 滴定浓度为0.1000 mol/L 的 HCl;以溴百里酚蓝为指示剂(pKa 为 7.1,变色范围 6.0 ∼ 7.6);计算指示剂在 ρ = 0.999 ∼ 1.001 范围内的浓度变化。
---
第五章
-分布分数
(虽然真的懒得记这个东西……但是玩意可能要考)
溶液中各级配合物存在的比例可以用分布分数来描述。

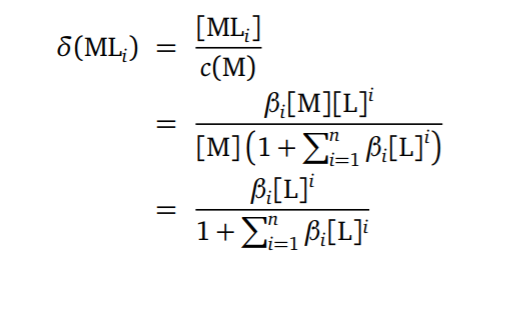

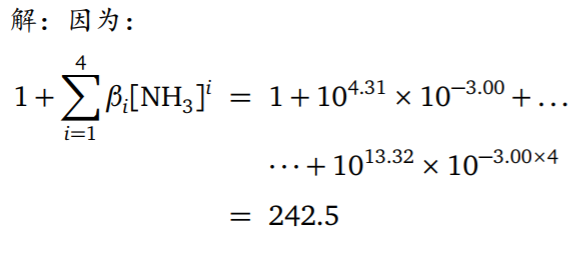

- 条件稳定常数
K′(MY) 是有副反应存在时 MY 的稳定常数,称为条件稳定常数。
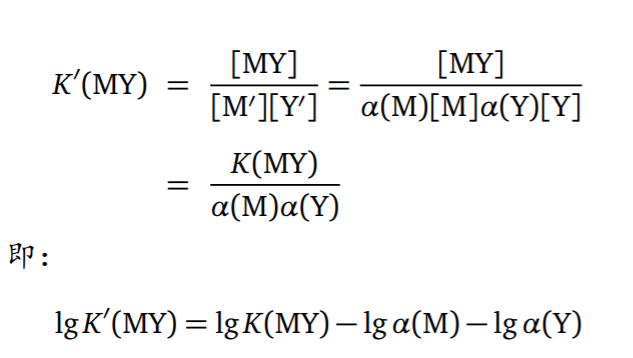





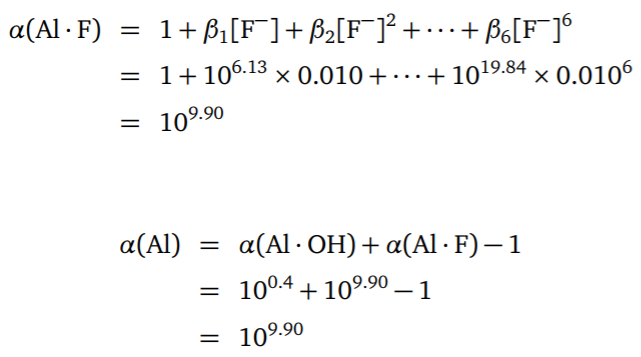

- 滴定方程的推导

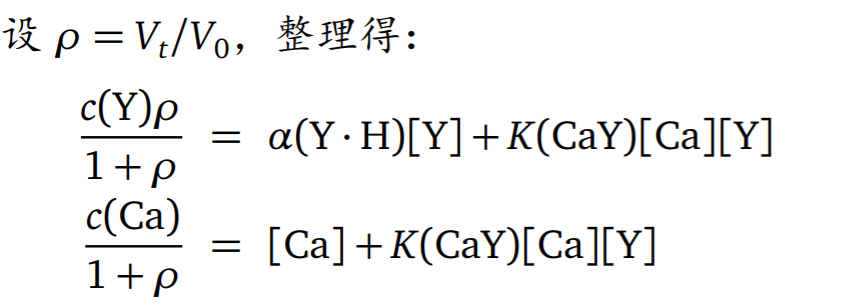
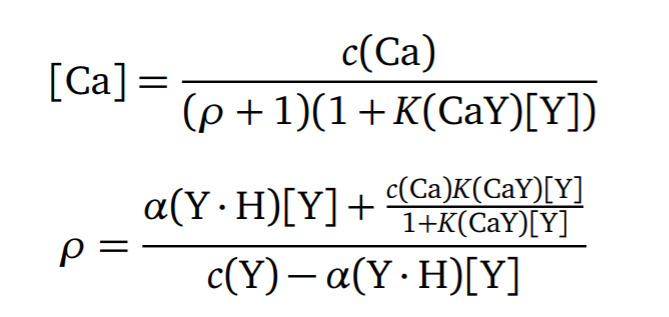
- 另一种表达形式
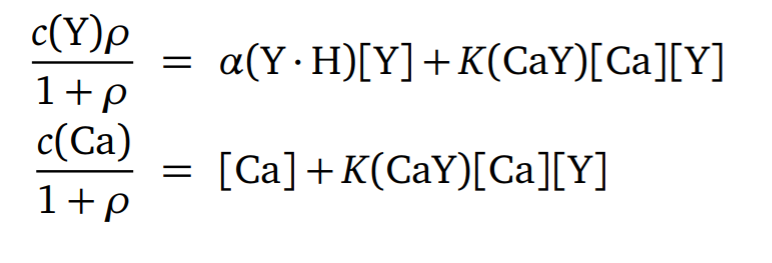
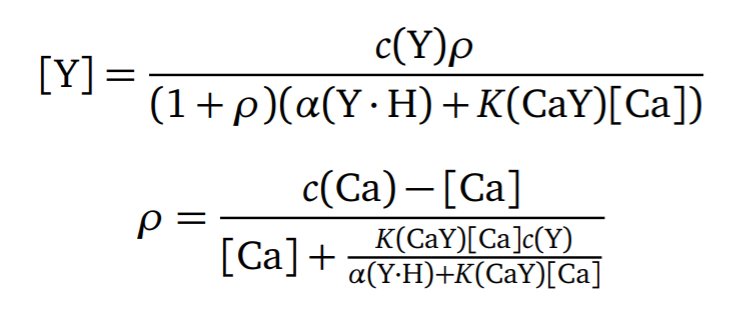

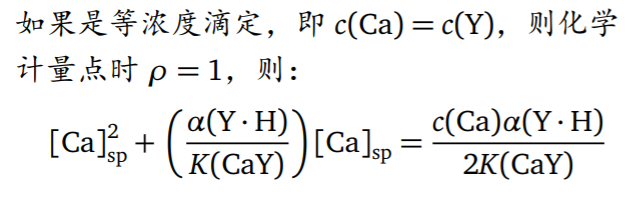
- 例题
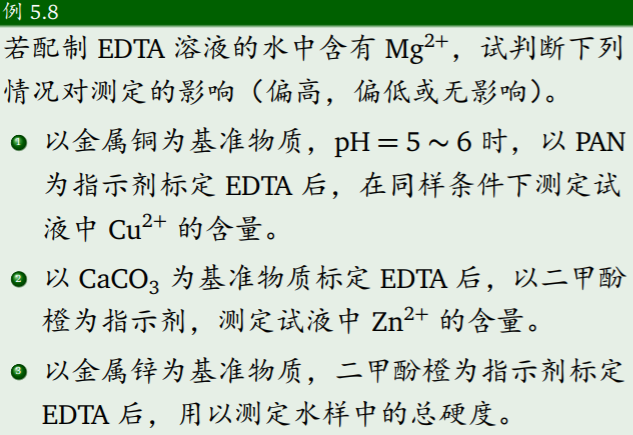



- 例题

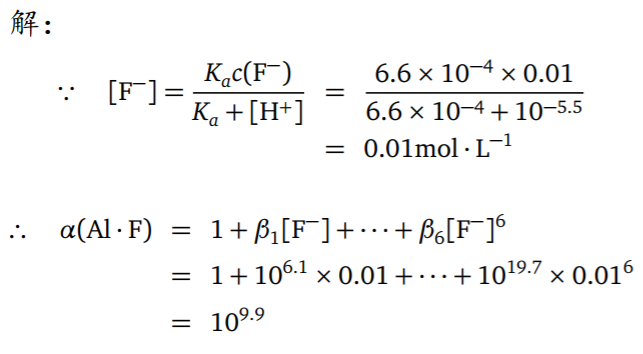

- 利用掩蔽法提高滴定的选择性
- 氧化还原掩蔽法
氧化还原掩蔽法是通过氧化还原反应改变干扰
离子的价态,使其与EDTA结合的能力降低,从而消除其对滴定过程的干扰。 - 沉淀掩蔽法
往金属离子的混合溶液中加入沉淀剂,利用沉淀反应降低干扰离子的浓度,在不分离沉淀的情况下,直接测定待测金属离子,这种消除干扰的方法称为沉淀掩蔽法。 - 氧化还原掩蔽法
氧化还原掩蔽法是通过氧化还原反应改变干扰离子的价态,使其与EDTA结合的能力降低,从而消除其对滴定过程的干扰。
- 氧化还原掩蔽法
- 沉淀掩蔽法的局限性
在实际的配位滴定分析中,沉淀掩蔽法用得并不多,原因有下面几个:
1 某些沉淀反应进行不完全,使得沉淀掩蔽不够完全;
2 生成沉淀的过程中往往发生共沉淀现象,因而影响滴定准确度。有时由于沉淀对指示剂的吸附作用,影响终点的观察;
3 如果沉淀本身有颜色或体积较大,会影响终点的观察。 - 配位滴定指示剂的一般原理
配位滴定指示剂是可与金属离子发生显色反应的有机试剂;
配位滴定指示剂与金属离子的稳定常数应略小于金属离子与 EDTA 的稳定常数。 配位滴定指示剂的选取原则
配合物 MIn 的颜色应与该指示剂In的颜色有显著的区别;
MIn 的稳定性应略小于MY配合物的稳定性指示剂与金属离子的反应必须迅速,并有良好的变色可逆性。
金属离子指示剂应较稳定,便于贮存和使用。



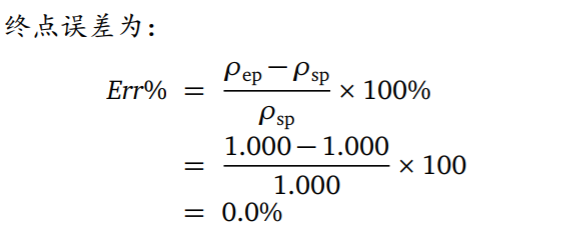




-常用的配位滴定方式直接滴定法
直接滴定法一般包括如下四个步骤:
1 将试样处理成溶液;
2 调节溶液的酸度至合适值;
3 加入其它必要的试剂(如辅助配位剂)和指示剂;
4 用 EDTA 标准溶液滴定待测的金属离子。
采用直接滴定法时,必须满足以下的条件:
反应能定量进行,且 lg c(M)K′(MY) ≥ 6;
配位反应速度要快;
应有合适的指示剂,且不会发生封闭现象;在滴定条件下,被测离子不发生水解和沉淀反应。返滴定法
返滴定法是在试液中先加入一定量的过量的
EDTA 标准溶液,过量的 EDTA 再用另一种金
属离子的标准溶液回滴。根据两种标准溶液的
浓度和用量,即可求得待测组分的含量。
返滴定法主要用于下列情形:
1 直接滴定时没有合适的指示剂,或待测离子对指示剂有封闭作用;
2 待测离子与 EDTA 的配位反应速度很慢;
3 待测离子在滴定条件下发生水解或沉淀反应,且没有合适的辅助配位剂。
例如,Al3+ 是一个典型的不能采用直接滴定法
的金属离子,原因如下:
Al3+ 对二甲酚橙等指示剂有封闭作用;
Al3+ 与 EDTA 配位反应速度在常温下很慢;
Al3+ 易水解生成一系列多核氢氧基配合物,导致 Al3+ 与 EDTA 反应缓慢,且配位比不稳定。
所以,滴定 Al3+ 时应采用返滴定法。首先,在Al3+溶液中加入一定量的过量的 EDTA 标准溶液,控制酸度在 pH ≈ 3.5,且煮沸溶液。在酸度较大的情况下,Al3+ 不易形成多核氢氧基配合物,在加热和 EDTA 过量的情况下,Al3+ 与EDTA 反应完全。置换滴定法
置换滴定法是通过置换反应,置换出另一种金
属离子,或者置换出EDTA,然后再进行滴定的一种配位滴定法。
置换滴定法常用于金属离子与EDTA形成的配合物不太稳定的场合,此时反应进行的程度不完全,无法直接定量。间接滴定法
有些金属离子和非金属离子不与 EDTA 反应,
或者生成的配合物很不稳定,此时可以采用间
接的方式利用配位滴定法来测定。
第六章
- 氧化还原滴定法
氧化还原滴定法是基于滴定剂和待测物之间的氧化反应实现定量分析的一种容量分析方法;
由于氧化还原反应的机制非常复杂,氧化还原滴定法需要很好地兼顾反应速度和反应平衡。 - 活度概念
活度是用于表征真实溶液中组分的浓度的量;
真实溶液的浓度越低,活度与浓度的值越接近。 - 表观电极电位

- 例题


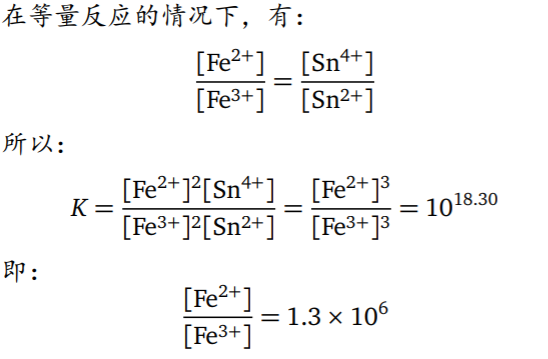
- 以浓度为变量的滴定方程
- 以电量为变量的滴定方程
(不写了……自己看去……) - 滴定方程的一般形式


- 终点误差


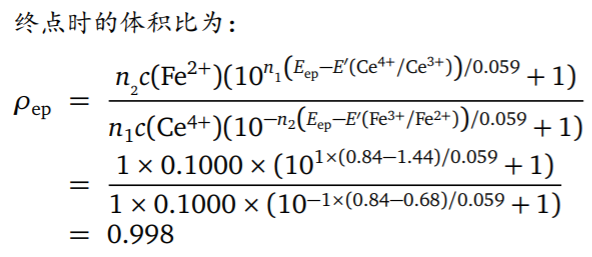
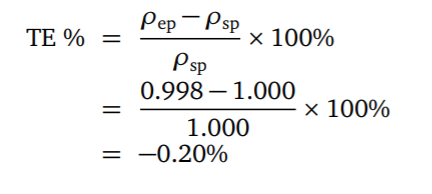
- 举例
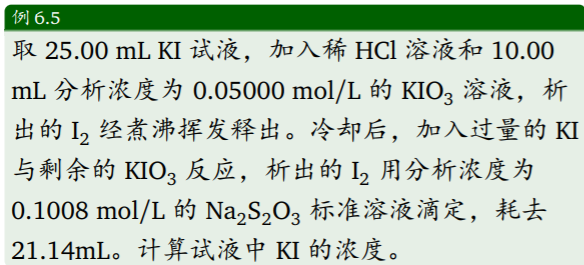




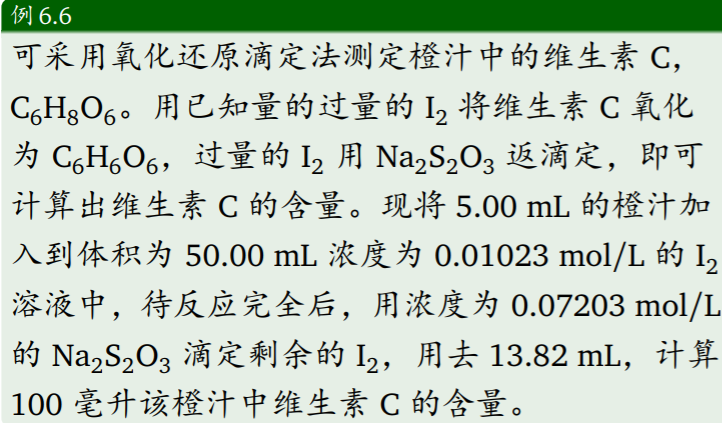



第七章
- 重量分析法
重量分析法是通过称重的方式对待测物进行定量分析的一类方法的统称。
重量分析法包括所有的以测量质量或质量改变为技术的方法。 - 沉淀重量分析法
沉淀法是将待测组分以微溶化合物的形式从试液中沉淀出来,再将沉淀过滤、洗涤、烘干或灼烧、称量,然后根据称量的形式求得待测组分的含量。 - 挥发重量分析法
挥发重量分析法是通过加热或其它方法使试样中的待测组分气化逸出,然后根据试样所减轻的重量,计算试样中该组分的含量;或者,当该组分逸出时,用吸收剂将其吸收,然后根据吸收剂重量的增加来计算该组分的含量。 - 电重量分析法
电解法是将金属离子在电极上析出,根据电极增加的重量,求得该组分的含量。 - 举例(一大波例子)

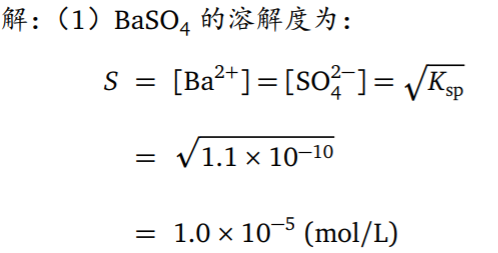
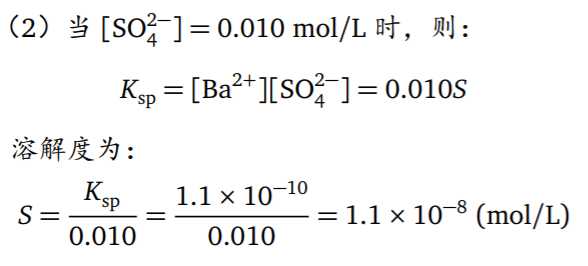



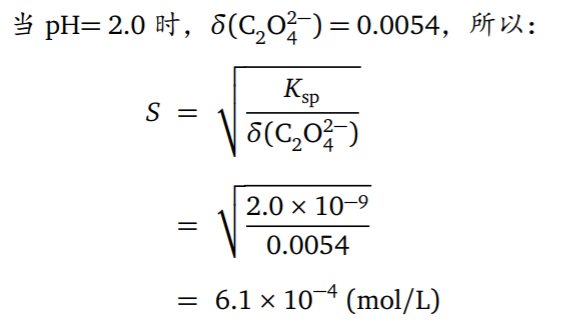


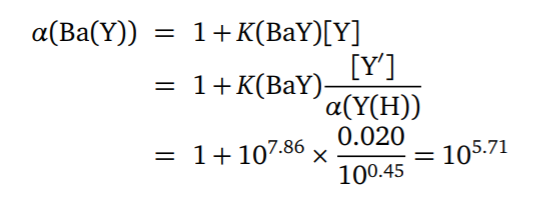
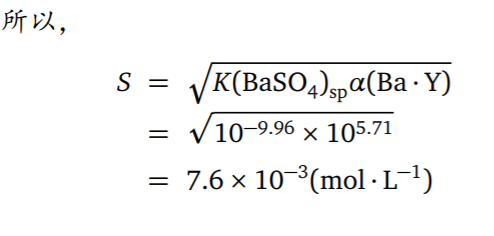





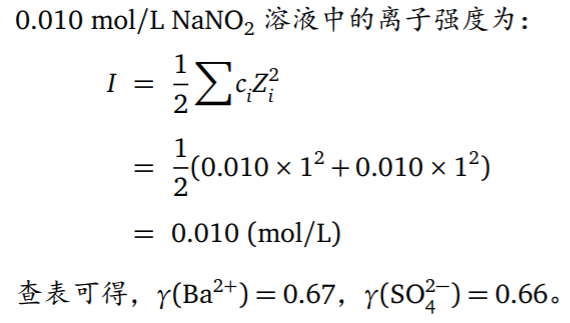
- 共沉淀
共沉淀是指沉淀过程中,某些可溶性杂质混杂在沉淀中一同沉积下来的现象。
产生共沉淀的原因有表面吸附、吸留和生成混晶。 - 后沉淀
沉淀析出之后,通常要在母液中存放一段时间,这一过程叫陈化,其目的是让小颗粒长成为大颗粒。
在陈化的过程中,溶液中的杂质离子会慢慢沉积到沉淀的表面上,这种现象称为后沉淀。 重量分析法对沉淀的要求
- 在试液中加入适当的沉淀剂,使被测组分以某种“沉淀形式”沉淀出来;
- 将沉淀过滤、洗涤后,再将其烘干或灼烧成“称量形式”进行称量,继而求得待测组分的含量。
对沉淀形式的要求
沉淀的溶解度要小,其溶解损失应不超过天平的称量误差;
沉淀应易于过滤和洗涤;
沉淀应有较高的纯度;
沉淀应易于转变为称量形式。- 对称量形式的要求
称量形式应具有确定的化学组成;
称量形式应稳定,不受空气中水分,二氧化碳等的影响;
称量形式应有较大的摩尔质量。 - 晶形沉淀的条件
- 沉淀应该在适当稀的溶液中进行,加入的沉淀剂浓度也要适当小,其目的在于使沉淀开始时溶液的相对过饱和度不会过大,产生的晶核也不会过多,以利于晶核的形成和长大;
- 应在搅拌下逐滴加入沉淀剂,这样可以防止局部过浓现象,以免产生大量的晶核;
- 沉淀作用应在热溶液中进行。热溶液会使沉淀的溶解度增加,减少沉淀表面吸附的杂质;
- 沉淀完成后,让沉淀在母液中陈化一段时间。
无定形沉淀的条件
- 沉淀过程应在较浓的溶液中进行,加入沉淀剂的速度可适当快些。浓度大时,离子的水合程度较小,得到的沉淀比较紧密。但浓度大时也会导致吸附的杂质增多,所以在沉淀完毕后,应加入大量热水稀释母液,并搅拌沉淀使吸附的杂质转入到溶液中;
- 沉淀过程应在热溶液中进行,这样不但可以防止生成胶体溶液,还可减少杂质的吸附,并使生成的沉淀紧密;
- 在溶液中加入适当的电解质,以防止生成胶体溶液。加入的电解质应易于加热除去;
- 沉淀作用完毕后应趁热过滤,而不必陈化。无定形沉淀长时间放置后易脱水,从而使沉淀变得很紧密,不利于后续的洗涤净化
过程; - 视具体情况,对沉淀进行再沉淀
常用的沉淀剂
常用的沉淀剂有无机沉淀剂和有机沉淀剂两类。有机沉淀剂与无机沉淀剂相比较,具有如下的优点:- 有机沉淀剂的品种多,可选范围广;
- 生成的有机沉淀的溶解度小,有利于待测组分沉淀完全;
- 沉淀对无机杂质的吸附量小,易于获得纯净的沉淀;
- 沉淀的相对分子量大,有利于提高分析的准确度。
有机沉淀剂也存在以下缺点: - 有机沉淀剂在水中的溶解度很小,易漂浮在溶液表面,给操作带来困难;
- 有些有机沉淀剂形成的沉淀的组成不恒定,依然需要通过灼烧的方式获得确定的称量形式。
剩下的自己看~
--- 祝考试顺利 ---
